Glicopeptidi
Generalità
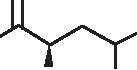
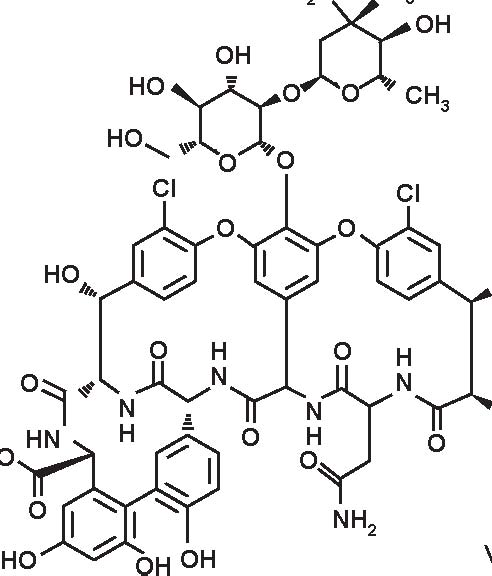
I due glicopeptidi attualmente usati in clinica, la vancomicina e la teicoplanina (Figura 1), sono degli antibiotici di uso esclusivamente ospedaliero, a somministrazione parenterale, impiegati nel trattamento delle gravi infezioni causate da cocchi Gram positivi multiresistenti e delle infezioni da Clostridium difficile (colite acuta pseudomembranosa). I lipopeptidi, un nuovo gruppo di antibiotici ad essi strettamente correlato, sono attualmente in fase di sviluppo.
Proprietà fisico-chimiche
I glicopeptidi sono antibiotici di estrazione, con struttura chimica complessa (peptidi macromolecolari triciclici), dielevato peso molecolare (1450-1490).La vancomicina è ottenuta a partire da colture di Streptomyces orientalis, mentre la teicoplanina è ottenuta apartire da colture di Actinoplanus theichomyceticus.
Spettro d'azione e resistenze batteriche
Lo spettro dei glicopeptidi è ristretto, molto simile per i due glicopeptidi, ed è limitato a cocchi e bacilli Gram positivi aerobi ed anaerobi: -Cocchi Gram positivi: Staphylococcus aureus, epidermidis, haemolyticus, meticillino-sensibili e meticillino-resi-
stenti; streptococchi, enterococchi (anche resistenti alle penicilline ed agli aminoglicosidi), pneumococchi a di-minuita sensibilità o francamente resistenti alla penicillina. -Bacilli Gram positivi: Corynebacterium JK, Propionibacterium, Eikenella, Listeria, Rhodococcus equii, Bacillus
anthracis. -Anaerobi Gram positivi: Clostridi, compresi C.difficile, peptococchi, actinomiceti. -Batteri resistenti sono: Nocardia, Leuconostoc, Erysipelothrix, cocchi e bacilli Gram negativi aerobi ed anaerobi
(Bacteroides, Fusobacterium), treponemi, micobatteri e tutti i batteri privi di parete cellulare. -Flavobacterium meningosepticum, nonostante sia resistente in vitro, si mostra sensibile in vivo. Esistono delle piccole differenze tra gli spettri antibatterici dei due glicopeptidi: la vancomicina è più attiva sugli stafilococchi coagulasi negativi (Staphylococcus haemolyticus), mentre la teicoplanina è più attiva sugli enterococchi e su E. faecium resistente alla vancomicina che su Listeria ed anaerobi Gram positivi. Sullo stafilococco aureo la loro azione è equivalente ma la teicoplanina mostra attività battericida più lenta. La resistenza batterica è di difficile insorgenza ed è ancora molto rara in Francia. Essa è stata descritta soprattutto per Staphylococcus haemolyticus (teicoplanina) ed Enterococcus faecium: resi-stenza ad entrambi i glicopeptidi per fenotipo Van A, o alla sola vancomicina per il fenotipo Van B, così come per i lattobacilli (resistenza plasmidica). Spesso, ma non sempre, si riscontra una resistenza crociata tra i due glicopeptidi; ad esempio, ceppi di stafilococchi coagulasi negativi resistenti alla teicoplanina restano spesso sensibili alla vancomicina. All'opposto, alcuni ceppi di
E. faecium, resistenti alla vancomicina, possono rimanere sensibili alla teicoplanina. Enterococchi resistenti ai glicopeptidi si repertano soprattutto negli USA, particolarmente tra gli immunodepressi ed i soggetti anziani. Esistono diversi fenotipi di resistenza ai glicopeptidi: -Fenotipo Van A: di resistenza di alto livello ad entrambi i glicopeptidi -Fenotipo Van B: resistenza alla sola vancomicina -Fenotipo Van C: resistenza di basso livello, non inducibile. Recentemente sono stati descritti ceppi di stafilococchi ed enterococchi “tolleranti” alla vancomicina (BMC > 32 volte la MIC). Il pH ottimale per l'attività antibatterica è quello neutro. Spesso si ha sinergia battericida con gli
H2N CH3
OH
O CH3
N HO
H
 HN
HN
 CH3
CH3
CH3
CH3
VANCOMICINA
H OH
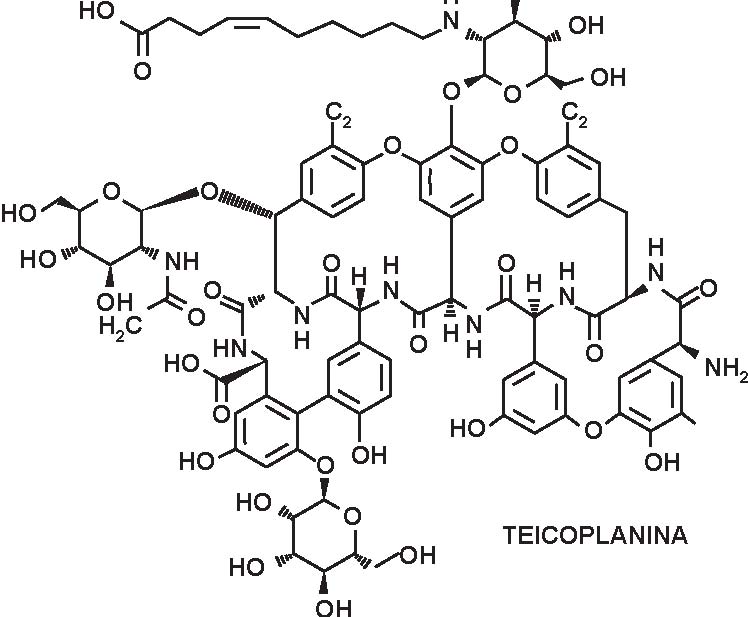
Figura 11.1 Formule di struttura.
aminoglicosidi, le streptogramine, la fosfomicina,
l'imipenem e le cefalosporine (stafilococchi, enterococchi); uneffetto
additivo o indifferente si ha con la rifampicina ed i fluorochinoloni;
talvolta con l'ampicillina si ha un effettoantagonista in vitro
sugli enterococchi.Per l'antibiogramma si utilizzano dischetti
impregnati con 30 mg di teicoplanina.
L'effetto inoculo è più importante con la teicoplanina che con la
vancomicina (soprattutto per S. epidermidis e S.haemolyticus).
Meccanismo d'azione
Inibizione della sintesi del peptidoglicano della parete batterica, ad uno stadio più precoce rispetto a quello dei beta-lattamici e più tardivo rispetto a quello della fosfomicina. La vancomicina agisce anche con altre modalità, alterando la permeabilità della membrana citoplasmatica batterica ed inibendo la sintesi dell'RNA batterico. I glicopeptidi possiedono azione di tipo battericida lenta, tempo-dipendente, sui batteri in fase di moltiplicazione attiva. Per gli enterococchi e Staphylococcus haemolyticus l'azione è piuttosto di tipo batteriostatico. L'effetto inoculo è più importante con la teicoplanina che con la vancomicina.
Farmacocinetica
Vancomicina
Dopo somministrazione di 1000 mg per perfusione endovenosa lenta si raggiungono picchi sierici di circa 23 mcg/ml (20-50)Dopo perfusioni ripetute i picchi sierici arrivano fino a 50 mcg/mlI tassi sierici residui, 6 ore dopo la perfusione, sono di circa di 10 mcg/ml.I tassi terapeutici utili durante il trattamento devono essere di 30-40 mcg/ml come picchi sierici e di 5-10 mcg/mlcome tassi residui; essi si ottengono con dosi quotidiane di 25-30 mg/kg/die, con una funzione renale normale.Dopo somministrazione intraperitoneale si ha un assorbimento in circolo del 50-65%.Per via orale, i due glicopeptidi non vengono assorbiti in caso di integrità della mucosa gastroenterica; tuttavia, uncerto assorbimento si verifica in caso di colite acuta pseudomembranosa o di insufficienza renale severa.
Teicoplanina
Dopo somministrazione endovenosa diretta (bolo) di 3 o 6 mg/kg i picchi sierici ammontano rispettivamente a 50 e110 mcg/ml; le concentrazioni plasmatiche residue 24 ore dopo la somministrazione sono rispettivamente di 4 ed 8mcg/ml. Dopo somministrazioni ripetute (400 mg ogni 12 ore) le concentrazioni residue raggiungono i 10 mcg/ml.Dopo somministrazione intramuscolo (200 mg) si ottengono picchi plasmatici di 12 mcg/ml e concentrazioni resi-due di 6 mcg/ml.L'emivita plasmatica è differente per i due glicopeptdi: 6-8 ore, ma con ampie variazioni individuali (3-9 ore) per lavancomicina; > 30 ore per la teicoplanina, con grandi variazioni individuali (tra 40 e 70 ore). L'emivita si allungaconsiderevolmente in caso di insufficienza renale; essa è invece accorciata nei neutropenici, negli ustionati, negliammalati di AIDS, nei tossicodipendenti per via endovenosa, nei neonati e nei bambini.L'AUC è di 300 mcg/h/l per la vancomicina e di 500 mcg/h/l per la teicoplanina.Il legame alle proteine plasmatiche e di circa il 55% per la vancomicina (altri autori affermano il 30%) e del 90-95%per la teicoplanina.Il volume di distribuzione è di 0.80-1.2 l/kg (40-60 l) per la teicoplanina e di 0.40-0.80 l/kg (30-50 l) per la vancomicina.La biotrasformazione metabolica è minima o del tutto assente per i due glicopeptidi (< 5%) i quali vengono elimi-nati nelle urine sotto forma attiva ed immodificati.La diffusione tissutale è buona nelle sierose pleurica, peritoneale, pericardica e sinoviale; variabile ed irregolare è ladiffusione nel liquor (meningi integre) e nell'umor acqueo, soprattutto per la teicoplanina. La teicoplanina sembrapossedere anche, grazie alla sua lipofilia, una diffusione intracellulare (intraleucocitaria).L'eliminazione biliare è ridotta.La clearance totale è di 98-110 ml/min/1.73 m2 per la vancomicina e di 12-20 ml/min/1.73 m2 per la teicoplanina.La clearance renale è di 75 ml/min per la vancomicina e di 7-8 ml/min per la teicoplanina.L'eliminazione renale avviene esclusivamente per filtrazione glomerulare.Per la vancomicina l'eliminazione urinaria è rapida: 80% nelle urine delle 24 ore; per la teicoplanina essa avvienepiù lentamente e prolungatamente (25-30 % nelle urine delle 24 ore).I tassi urinari sono di 400-800 mcg/ml per la vancomicina e di 20-100 mcg/ml per la teicoplanina; entrambi iglicopeptidi non sono dializzabili o lo sono molto poco.
Tossicità ed effetti indesiderati
Tra i due glicopeptidi vi sono alcune differenze in favore della teicoplanina per quanto concerne la frequenza e la gravità di alcuni effetti indesiderabili. Tuttavia, per quanto riguarda la vancomicina, la frequenza di tali effetti è nettamente diminuita da quando viene utilizzata un prodotto cromatograficamente molto più purificato rispetto alle vecchie preparazioni. L'intolleranza locale a livello venoso (flebite, tromboflebite) si verifica soprattutto con la vancomicina (10 %, dei casi), la cui soluzione ha un pH acido; essa, d'altronde, va somministrata solo in perfusione lenta e mai in bolo in quanto v'è il rischio di arresto cardiaco. Al fine di ridurre al minimo le reazioni locali venose, devono essere intraprese alcune misure: la soluzione deve essere sufficientemente diluita (in 200-250 ml di fisiologica o di glucosata isotonica), deve essere somministrata lentamente (in 1-2 ore) evitando ogni stravaso; la perfusione andrebbe fatta di preferenza attraverso un catetere centrale (sottoclavicolare) oppure, nel caso venga effettuata in una vena periferica, bisogna alternare i punti di infusione. La perfusione lenta sufficientemente diluita è anche in grado di evitare o comunque di ridurre la sindrome caratte-rizzata da flush al volto (arrossamento diffuso), al collo ed alle spalle detta “sindrome dell'uomo rosso” (“red man syndrome”), accompagnata da prurito, orticaria, ipotensione arteriosa ed, eccezionalmente, convulsioni. Il meccani-smo di questa sindrome è dovuto alla liberazione di istamina; essa può esere prevenuta o attenuata dalla somministrazione di antistaminici prima di effettuare la perfusione della vancomicina, che deve essere lenta (2 ore). La teicoplanina sembra causare molto più raramente sia la sindrome dell'uomo rosso che gli effetti collaterali locali venosi, in quanto la sua soluzione ha pH neutro. Reazioni allergiche quali febbre, eruzioni cutanee, orticaria, broncospasmo, lacrimazione e reazioni anafilattiche, possono verificarsi con ambedue gli antibiotici; tuttavia, esse sono divenute più rare in seguito all'utilizzo di pro-dotti più purificati. Una ototossicità, a predominanza cocleare, di tipo dose-dipendente, irreversibile, in stretta relazione a tassi pla-smatici eccessivi (superiori a 50 mcg/ml), può riscontrarsi con la vancomicina soprattutto, associata agli aminoglicosidi; fattori favorenti sono costituiti, oltre che dagli eccessivi tassi plasmatici, da trattamenti prolungati, dall'età avan-zata e dall'insufficienza renale. La prevenzione consiste nell'evitare la vancomicina nei soggetti che hanno già deficit uditivi, nel monitorare con l'esame audiometrico i soggetti trattati, nei quali va anche controllata la funzio-nalità renale, e nel controllare i tassi plasmatici di vancomicina, soprattutto in caso di trattamenti prolungati. Occorre sospendere la vancomicina in caso di comparsa di acufeni in quanto questi costituiscono un prodromo della sordità. La nefrotossicità (nefropatia tubulo-interstiziale) si manifesta soprattutto con modificazioni urinarie e con eleva-zione della creatininemia e della enzimuria. Fattori favorenti sono dosi elevate, trattamenti prolungati, età avanzata, associazione con altri antibiotici o altri farmaci nefrotossici: amfotericina B, aminoglicosidi, ciclosporina, cisplatino, diuretici dell'ansa. Contrariamente all'ototossicità, la nefrotossicità non sembra essere in relazione con tassi plasmatici eccessivi: la prevenzione si basa su una ottimale posologia del farmaco adattandone le dosi in funzione della creatininemia. Alcuni autori raccomandano l'associazione con la fosfomicina che, sperimentalmente, diminuisce la nefrotossicità della vanco-micina. La nefrotossicità è nettamente più ridotta con la teicoplanina che con la vancomicina. Una eosinofilia ed una neutropenia, che eccezionalmente può arrivare fino alla agranulocitosi, possono riscontrarsi raramente (2%), soprattutto in caso di trattamenti prolungati per più di 2 settimane con vancomicina e con dosi elevate (più di 10 mg/kg/die) con la teicoplanina; più rara è una trombocitopenia. La neutropenia è probabilmente di origine immunologica, benché l'insufficienza renale possa costituire un suo fattore scatenante; essa deve essere prevenuta con un'attenta sorveglianza ematologica e, tuttavia, è il più delle volte reversibile alla sospensione del trattamento. Qualche volta, un soggetto che ha presentato leucopenia con la vancomicina può comunque essere ulteriormente trattato con la teicoplanina. Alcuni autori hanno suggerito una sensibilità crociata ai glicopeptidi ed alle beta-lattamine da parte delle cellule ematopoietiche del midollo osseo. Disturbi gastroenterici quali nausea, vomito e diarrea si riscontrano soprattutto dopo somministrazione orale. È stato descritto un aumento delle transaminasi e della fosfatasi alcalina in seguito a somministrazione di teicoplanina.
Indicazioni cliniche
Gli attuali glicopeptidi, di uso esclusivamente ospedaliero, sono degli antibiotici da impiegare solamente nelle gravi infezioni nosocomiali da germi Gram positivi multiresistenti: stafilococchi meticillino- ed aminoglicosido-resistenti
(S. aureus, S. epidermidis, S. haemolyticus), enterococchi e pneumococchi resistenti alle beta-lattamine (soprattut-to in caso di meningite), Streptococchi resistenti, endocarditi da Corynebacterium, o nei soggetti allergici alle beta-lattamine. Per os vengono impiegati nel trattamento delle coliti acute pseudomembranose da Clostridium difficile, sebbene le ricadute cliniche o semplicemente batteriologiche siano relativamente frequenti alla sospensione del trattamento. Per prevenire le ricadute, è stato proposto un trattamento sequenziale con somministrazione di lieviti o lattobacilli dopo quella di glicopeptidi. I batteri isolati nel corso di queste ricadute restano tuttavia sensibili in vitro ed in vivo ai glicopeptidi. Più recentemente è stato proposto il trattamento con glicopeptidi per os per la decontaminazione batterica del tubo gastroenterico (in associazione ad altri antibiotici non assorbiti per os) nei pazienti aplasici. Per via parenterale questi antibiotici vengono usati soprattutto nel trattamento delle setticemie, delle endocarditi, delle meningiti, delle peritoniti insorte come complicanza della dialisi peritoneale ambulatoriale continua; essi vengono anche impiegati nel trattamento delle infezioni osteoarticolari (buona diffusione intraossea), in associa-zione ad altri antibiotici a buona diffusione ossea, quali l'acido fusidico, i fluorochinoloni e la rifampicina. La teicoplanina è soprattutto indicata quando si è di fronte ad una riduzione del circolo venoso e come switch terapy ambulatoriale nei pazienti trattati in ospedale con vancomicina, in ragione della sua maggiore praticità d'uso. Entrambi i glicopeptidi sono utilizzati come profilassi dell'endocardite batterica nei soggetti portatori di protesi valvolare ed in chirurgia dentaria (estrazioni), qualora si sospetti come agente causale uno stafilococco o un enterococco multiresistenti, oppure in caso di allergia ai betalattamici.
Controindicazioni e precauzioni d'uso
Controindicazioni: precedenti di ipersensibilità ai glicopeptidi.
Precauzioni d'uso: adattare la posologia nei pazienti con insufficienza
renale, in ragione dei valori di creatininemia.
In caso di trattamento prolungato e di associazione con altri farmaci
aventi effetti collaterali simili, occorre moni
torare le funzioni ematica, renale ed uditiva, nonché i tassi plasmatici
dell'antibiotico.
Interazioni farmacologiche
Interazioni utili (Tabella 11.1) -Con gli aminoglicosidi: stafilococchi, enterococchi multiresistenti (ma esiste un aumentato rischio di nefrotossicità ed ototossicità) -Con rifampicina, acido fusidico, fosfomicina, beta-lattamine antistafilococciche, fluorochinoloni, streptogramine, clindamicina, trimethoprim: stafilococchi meticillino-resistenti -Con aminopenicilline, ureidopenicilline, imipenem: enterococchi multiresistenti -Con preparati a base di Sacharomyces cerevisiae, nella prevenzione e nel trattamento delle recidive di colite
pseudomembranosa dopo una terapia con glicopeptide o metronidazolo. Interazioni da evitare (Tabella 11.2) -Con altri farmaci in grado aumentare la nefrotossicità e l'ototossicità: amfotericina B, ciclosporina, polimixina-
colistina, cisplatino, diuretici dell'ansa, pentamidina, foscarnet -Con la colestiramina, in caso di somministrazione orale del glicopeptide: distanziare i due farmaci di almeno tre ore, al fine di evitare la perdita di attività antibatterica del glicopeptide.
Modalità di somministrazione e posologia
Vancomicina: fiale da 500 mg e 1 g per infusione endovenosa lenta; tale formulazione può essere somministrata anche per via orale nelle enterocoliti stafilococciche e nella colite pseudomembranosa da Clostridium difficile causata da antibioticoterapia. Per queste indicazioni sono disponibili anche capsule da 250 mg. Teicoplanina: flaconi con 200 mg di liofilizzato + 3 ml di solvente (acqua per preparazioni iniettabili); questi posso-no essere iniettati direttamente in vena (bolo) o possono essere diluiti in fisiologica o glucosata e perfusi lentamen-te in vena. Posologia giornaliera: -Vancomicina: 2 grammi/die (30 mg/kg/die) nell'adulto, ripartiti in 500 mg ogni 6 ore o in 1000 mg ogni 12 ore, in
perfusione lenta di almeno un'ora per evitare la sindrome da flushing e gli effetti collaterali locali venosi. In caso d'insufficienza renale, adattare la posologia in funzione della creatininemia e controllare le concentrazioni plasmatiche della vancomicina (picco e valle). Cambiare continuamente il punto di iniezione. Nei soggetti neutropenici sono spesso necessarie posologie più elevate (> 2 grammi/die). Nei bambini 40 mg/kg/die, suddivisi in 10 mg/kg/die ogni 6 ore in perfusione endovenosa lenta. Per via endorachidea si somministrano 20-30 mg di vancomicina. Per via intraperitoneale, si impiega la vancomicina aggiunta al liquido di dialisi ad una concentrazione di 20-50 mg/l, in associazione ad un aminoglicoside, nella terapia delle peritoniti insorte come complicanza della dialisi peritoneale ambulatoriale continua (CAPD). La posologia per via orale negli adulti è di 500-2000 mg/ die, ripartiti in quattro assunzioni quotidiane, per 10 giorni (nella colite acuta pseudomembranosa). Nei bambini la posologia è di 40 mg/kg/die, in 3-4 assunzioni. Nei pazienti sottoposti ad emodialisi si somministra un grammo di vancomicina ogni 7-10 giorni, controllandone i tassi sierici.
-Teicoplanina: per gli adulti è necessario somministrare, in prima giornata, 6 mg/kg/die (400 mg) per via ev; nei giorni successivi 6 mg/kg/die (400 mg) per via ev o 3 mg/kg/die (200 mg) per via ev o im, in somministrazione unica nella giornata; dosaggi più alti si raccomandano per le infezioni gravi. Per i bambini la posologia è di 10 mg/ kg ogni 12 ore per un totale di 3 dosi seguite da 6-10 mg/kg/die. Si raccomanda la somministrazione della teicoplanina direttamente in vena, soprattutto nei tossicodipendenti, i quali presentano tasasi sierici più bassi ed un'emivita più breve. Si raccomanda, al momento della preparazione della soluzione, di introdurre lentamente il solvente nel flacone, al fine di evitare la formazione di schiuma. Durante il trattamento, le concentrazioni sieriche residue non dovranno essere inferiori a 10 mcg/ml ed i picchi sierici non dovranno oltrepassare i 50 mcg/ml. Come profilassi in chirurgia dentaria, si impiegano 400 mg di teicoplanina al momento di induzione dell'anestesia. In caso d'insufficienza renale, ridurre la posologia quotidiana dei glicopeptidi, dato l'allungamento della loro emivita.
Antibiotici o Indicazioni altri farmaci Tipo di effetto Meccanismo principali
Acido fusidico
Beta-lattamine antistafilococciche: penicilline antistafilococciche, cefalosporine di I generazione
Aminopenicilline, ureidopenicilline, amossicillina-acido clavulanico
Cefalosporine di III e IV generazione
Imipenem, meropenem
Monobattamici (aztreonam)
Aminoglicosidi
Clindamicina
Fluorochinoloni
Fosfomicina
Sinergia o effetto additivo antibatterico + inibizione delle resistenze batteriche + buona diffusione ossea (acido fusidico)
Sinergia antibatterica; inibizione delle resistenze batteriche
Sommazione degli effetti antibatterici (enterococchi, anaerobi)
Sinergia antibatterica; inibizione delle resistenze batteriche + ampliamento dello spettro antibatterico
Sinergia antibatterica; inibizione delle resistenze batteriche
Ampliamento dello spettro antibatterico + inibizione delle resistenze batteriche. Evitamento delle sovrainfezioni da cocchi Gram positivi
Sinergia battericida; tuttavia aumento del rischio di oto- e nefrotossicità, soprattutto con la vancomicina
Sinergia o effetto additivo antibatterico; inibizione delle resistenze batteriche
Effetto additivo o sinergia antibatterica; inibizione delle resistenze batteriche
Sinergia antibatterica; forse anche diminuzione della nefrotossicità della vancomicina; inibizione delle resistenze batteriche Azione antibatterica a due livelli differenti: parete batterica (glicopeptidi), inibizione della sintesi proteica batterica (acido fusidico)
Inibizione della sintesi della parete batterica a due livelli successivi
Inibizione della sintesi della parete batterica a due livelli successivi
Inibizione della sintesi della parete batterica a due livelli successivi
Inibizione della sintesi della parete batterica a due livelli successivi
Prevenzione delle sovrainfezioni da cocchi Gram positivi. Inibizione della sintesi della parete batterica a due livelli successivi. Evitamento delle reazioni allergiche alle altre betalattamine
Battericidi a due diversi livelli: parete batterica (glicopeptidi), aumentando la permeabilità di parete agli aminoglicosidi, che poi inibiscono la proteosintesi batterica
Inibizione batterica a due differenti livelli: parete batterica (glicopeptidi), proteosintesi batterica (clindamicina)
Inibizione batterica a due differenti livelli: DNA batterico (fluorochinoloni), parete batterica (glicopeptidi)
Inibizione della parete batterica a due livelli successivi Stafilococchi meticillino-resistenti (soprattutto in caso di localizzazione osteo-articolare); aerobi. Per via orale: colite da
Clostridium difficile
Stafilococchi, anche meticillino-resistenti
Enterococchi, anaerobi (ureidopenicilline, amossicillina-clavulanato)
Stafilococchi, pneumococchi a diminuita sensibilità alla penicillina (menigiti); infezioni miste da aerobi-anaerobi
Stafilococchi, enterococchi, anaerobi
Cocchi Gram positivi, Pseudomonas (terapia delle infezioni nei soggetti neutropenici allergici alle altre beta-lattamine)
Stafilococchi, enterococchi,
E. faecium
Stafilococchi, anaerobi
Stafilococchi (soprattutto le localizzazioni osteo-articolari); enterococchi, pneumococchi a diminuita sensibilità alla penicillina (sparfloxacina)
Stafilococchi meticillinoresistenti, pneumococchi a ridotta o assente sensibilità alla penicillina, enterococchi
(continua)
| Antibiotici o | Indicazioni | ||
| altri farmaci | Tipo di effetto | Meccanismo | principali |
| Minociclina | Sinergia antibatterica (stafilococchi meticillino-resistenti; inibizione delle resistenze batteriche) | Inibizione batterica a due differenti livelli: parete batterica (glicopeptidi), proteosintesi batterica (minociclina) | Stafilococchi meticillinoresistenti |
| Rifampicina | Sinergia o effetto additivo antibatterico; inibizione delle resistenze batteriche | Inibizione batterica a due livelli differenti: parete batterica (glicopeptidi), RNA batterico (rifampicina) | Stafilococchi meticillinoresistenti, pneumococchi a diminuita sensibilità (o resistenti) alla penicillina, enterococchi, anaerobi |
| Streptogramine | Sinergia o effetto additivo antibatterico; inibizione delle resistenze batteriche | Inibizione batterica a due livelli differenti: parete batterica (glicopeptidi), sintesi proteica batterica (streptogramine) | Stafilococchi meticillino-resistenti, pneumococchi a diminuita sensibilità (o resistenti) alla penicillina, E. faecium (quinopristina, dalfopristina) |
| Trimetoprim | Sinergia o effetto additivo antibatterico; inibizione delle resistenze batteriche | Inibizione batterica a due livelli differenti: parete batterica (glicopeptidi), azione antifolinica | Stafilococchi, enterococchi |
| (trimethoprim) | |||
| Preparazioni a base di lieviti (Saccaromyces cerevisiae) | Prevenzione e trattamento delle ricadute della colite da Clostridium difficile | Inibizione della selezione di Clostridium difficile | Profilassi e trattamento delle ricadute delle coliti post-antibiotiche dovute a selezione di Clostridium difficile (in associazione o in alternativa ai glicopeptidi) |
| Antibiotico | Altri antibiotici o altri farmaci | Tipo di rischio | Fattori favorenti | Meccanismo | Mezzi di prevenzione o correzione | Comportamento da adottare |
|---|---|---|---|---|---|---|
| Glicopeptidi | Amfotericina B | Aumento di nefrotossicità (soprattutto con vancomicina) | Insufficienza renale | Sommazione delle rispettive nefrotossicità | Monitorare creatininemia e tassi plasmatici dei glicopeptidi; adattare la posologia | Associazione da adottare con cautela |
| Aminoglicosidi | Aumentato rischio di nefrotossicità ed ototossicità (soprattutto con vancomicina), nonostante la sinergia antibiotica | Dosi elevate, trattamenti prolungati, insufficienza renale | Sommazione delle rispettive nefrotossicità | Monitorare creatininemia e tassi plasmatici degli aminoglicosidi; adattare la posologia | Associazione da adottare con cautela | |
| Aciclovir (soprattutto vancomicina) | Aumentato rischio di nefrotossicità | Insufficienza renale, dosi elevate (vancomicina) | Sommazione delle rispettive nefrotossicità | Monitorare la creatininemia | Associazione da adottare con cautela | |
| Polimixina B-colistina (soprattutto vancomicina) | Aumentato rischio di nefrotossicità | Dosi elevate, trattamenti prolungati, insufficienza renale | Sommazione delle rispettive nefrotossicità | Monitorare la creatininemia | Associazione sconsigliata | |
| Foscarnet (soprattutto vancomicina) | Aumentato rischio di nefrotossicità | Dosi elevate, trattamenti prolungati, insufficienza renale | Sommazione delle rispettive nefrotossicità | Monitorare creatininemia; adattare le posologie | Associazione da adottare con cautela | |
| Pentamidina (soprattutto vancomicina) | Aumentato rischio di nefrotossicità | Dosi elevate, trattamenti prolungati, insufficienza renale | Sommazione delle rispettive nefrotossicità | Monitorare creatininemia; adattare le posologie | Associazione da adottare con cautela | |
| Ciclosporina | Aumentato rischio di nefrotossicità | Insufficienza renale | Sommazione delle rispettive nefrotossicità | Monitorare creatininemia, ciclosporinemia; adattare le posologie | Associazione da adottare con cautela | |
| Cisplatino, carboplatino (soprattutto vancomicina) | Aumentato rischio di nefrotossicità | Insufficienza renale | Sommazione delle rispettive nefrotossicità | Monitorare creatininemia e tassi plasmatici dei glicopeptidi | Associazione da adottare con cautela | |
| Diuretici dell’ansa | Aumentato rischio di nefrotossicità ed ototossicità | Insufficienza renale | Potenziamento della nefrotossicità ed ototossicità | Monitorare creatininemia ed audiometria | Associazione da adottare con cautela (continua) |
GLICOPEPTIDI 299 300
| Antibiotico | Altri antibiotici o altri farmaci | Tipo di rischio | Fattori favorenti | Meccanismo | Mezzi di prevenzione o correzione | Comportamento da adottare |
|---|---|---|---|---|---|---|
| Desametasone | Diminuzione | Diminuzione della | Associazione da evitare | |||
| dell’attività dei | diffusione dei | |||||
| glicopeptidi (meningiti) | glicopeptidi nel liquor | |||||
| Analgesici morfinici (tossicodipendenti) | Rischio d’inefficacia terapeutica | Tossicodipendenti per via ev; ammalati di AIDS; posologia insufficiente | Diminuzione dei tassi plasmatici, dell’emivita ed aumento della clearance totale e | Monitorare i tassi sierici di teicoplanina; aumentare la sua posologia giornaliera | Associazione da valutare | |
| renale | ||||||
| Colestiramina | Diminuzione | Assunzione simultanea | ||||
| dell’assorbimento gastroenterico dei glicopeptidi | Soppressione del circolo entero-epatico dei glicopeptidi da parte della colestiramina | Intervallare l’assunzione dei due farmaci di almeno 3 ore | Associazione da valutare |